病毒的广泛存在
人们发现病毒的历史可以追溯到1892年发现烟草花叶病毒,但实际上病毒的历史却比人类的历史更加久远。病毒广泛分布在自然界中,无论是动物、植物、真菌、细菌等,都有其对应的病毒。

图1:A病原体图(图源自网络);B灵长类图(图源自网络);C灵长类和其已知的病原体分布图,蓝色代表丰度较低,红色代表丰度较高(图修订自参考文献[1])
灵长类类动物主要分布在热带与亚热带地区,这些地区同时也是病毒等病原体分布丰富的地区。因此灵长类动物的演化历史一直都伴随着与病毒的“相爱相克”。
宿主与病原体之间的“世纪较量”
病毒除了具有体积微小不易被察觉的特点之外,还具有更加令人吃惊的“本领”:病毒会在与宿主长期共存的攻防战中不断演化。病毒与宿主的长期共存涉及到一个演化概念:“协同演化”。“协同演化”是指两个相互作用的物种在进化过程中发展的相互适应的共同进化。举例来说,病毒需要与宿主体内的受体蛋白结合,从而感染宿主细胞。就像新型冠状病毒是通过与人体的ACE2蛋白结合来侵入细胞。宿主受体蛋白的“演化策略”是通过改变氨基酸序列来避免病毒的结合;反过来,病毒的“演化策略”是通过改变自身结合蛋白的氨基酸序列来保证结合。这是一场分子世界的“军备竞赛”(图2)。
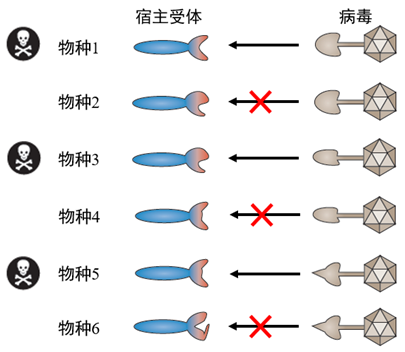
图2.宿主受体蛋白与病毒的“军备竞争”,箭头代表可以侵染,叉号表示无法侵染(图修订自参考文献[2])
中东呼吸综合征冠状病毒(MERS-CoV)于2012年被发现,人们鉴定出MERS-CoV的主要宿主受体为DPP4蛋白。在对抗MERS-CoV病毒的“战斗”中,不同的物种表现出不同的特点。在DPP4蛋白的结构域中,存在5个关键位置的氨基酸,这些氨基酸决定着宿主对MERS-CoV的抗感染能力。与人类相比,在仓鼠的DPP4结构域中出现了5个氨基酸位置的突变,使得MERS-CoV失去了与仓鼠DPP4结合的能力,仓鼠因此“获得了”对MERS-CoV较强的抗感染能力。但灵长类动物中,这5个氨基酸位置与仓鼠不同,MERS-CoV可以与灵长类(包括人)的DPP4结构域结合,所以灵长类动物的抗感染能力较差(图3)。
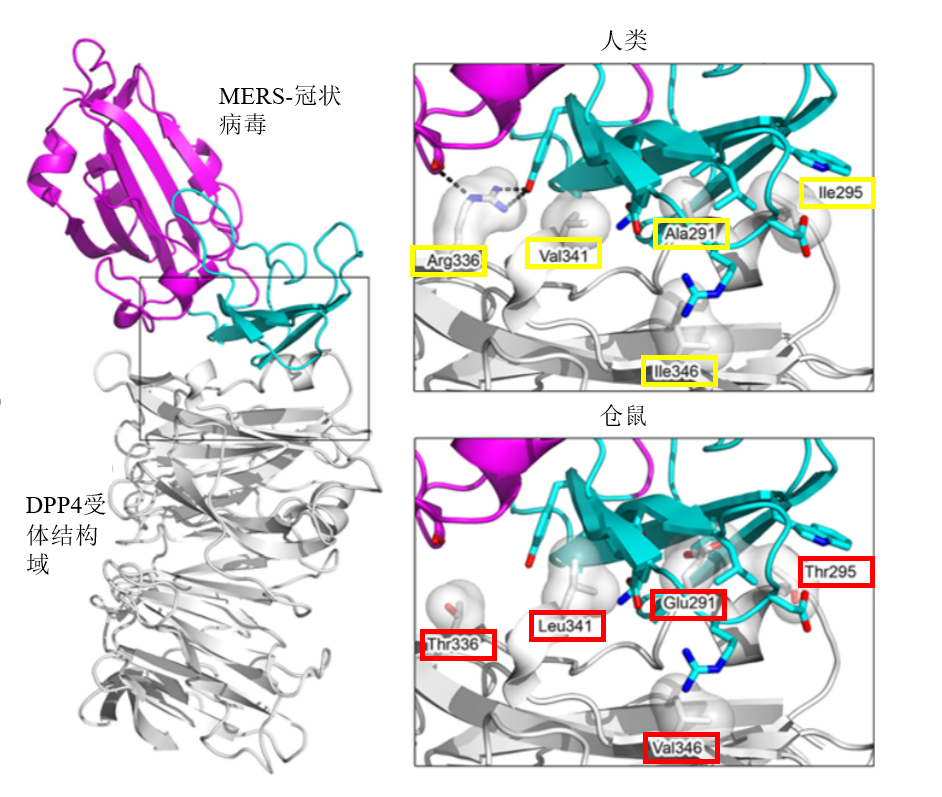
图3.MERS-CoV与DPP4蛋白(图修订自参考文献[3])
人类与病毒之间进化的“军备竞争”
宿主与病毒之间频繁的“冲突”就导致了两者间的“军备竞赛”。一方面宿主受体蛋白不断突变以提升对病毒的抵抗力,另一方面,病毒则努力“制定政策”改变自身从而实现对宿主的成功感染,因此宿主和病毒之间就会发生周期性的适应与反适应。这种现象通常被称为“红皇后”场景。这个有点“文艺”色彩的说法来自英国童话《爱丽丝梦游仙境》。红皇后对爱丽丝答道:“在这个国度中,必须不停地奔跑,才能使你保持在原地。”美国芝加哥大学进化生物学家范瓦伦()1973年提出了这个颇有哲学色彩的假说,恰如其分地描绘了自然界中的协同演化现象。这种规律也具有一定现实作用,如果一类宿主的受体蛋白发现了可以检测到的适应性演化现象,说明它们可能受到过或正在受到某种病毒的侵染。研究者曾通过对蝙蝠的ACE2蛋白的适应性演化研究,预测了蝙蝠可能是SARS病毒的宿主之一,这个预测也被后来的实验研究所证明。
病毒会“爱上”哪些宿主蛋白呢?
病毒蛋白数量很少,对宿主体内进行无差别的攻击是不现实的。实验表明,病毒对人类蛋白相互作用是通过有针对的攻击实现的(图4)。那么病毒攻击的目标又有哪些特点呢?研究人员发现,病毒进行“精确攻击”的受体蛋白主要具有以下特点:1.演化速率慢(慢);2.在多个器官组织广泛大量表达(多);3.缺乏稳定的三维结构(乱)。这些特点都会增加病毒与其结合的可能性。这个也容易理解:演化速率较慢的蛋白相对保守,一般是功能重要的蛋白,参与机体内的多个途径,在多个组织中大量存在,构象灵活。病毒侵入宿主体内后,这类广泛表达(到处有)且变异较慢(跑得慢)的蛋白容易被病毒“骚扰”,因而容易被病毒作为攻击目标。
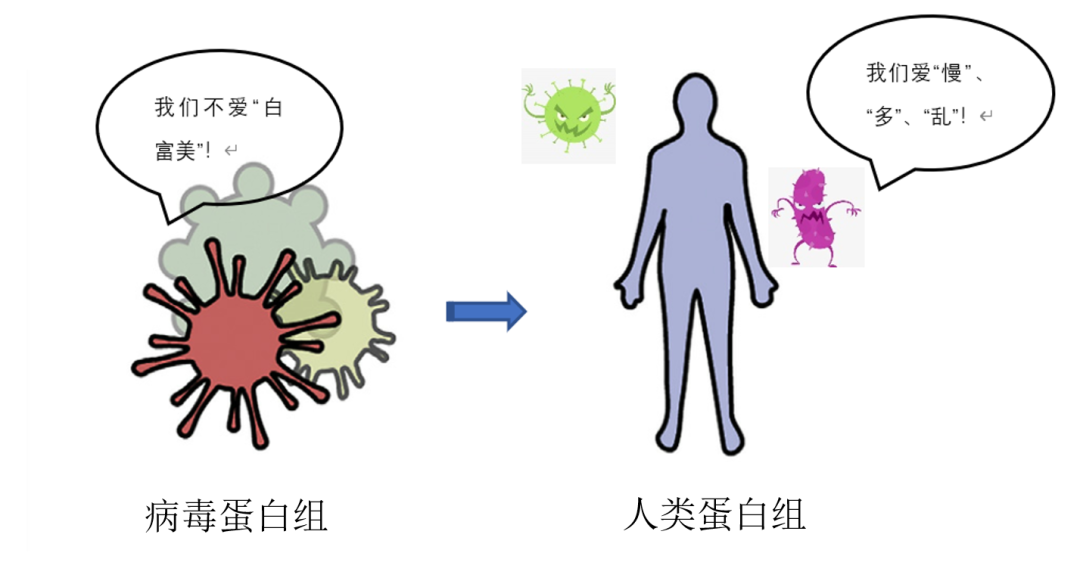
图4.病毒蛋白组与人类蛋白组(图修订自参考文献[4])
宿主抵抗病毒的防线
那么面对病毒的侵入,宿主就只能束手无策吗?答案当然是“不”!
在病毒侵入宿主之后,宿主体内有检测和对抗病毒的机制。例如Toll样受体(TLR)是对病原体受体进行识别的蛋白家族。在哺乳动物的TLR蛋白家族中有4个成员与病毒核酸的识别有关:TLR3、TLR7、TLR8、TLR9(图5)。

图5.TLR受体蛋白家族(图修订自参考文献[5])
克里米亚-刚果出血热是一种由布尼亚病毒科成员病毒引起的一种人类致死率极高的急性疾病。这种疾病通常会通过蜱虫叮咬传播给人类。人体中的TLR8和TLR9有助于识别该病毒,并引起机体内相应的免疫反应。研究者发现,当TLR8氨基酸序列中第1位的缬氨酸(Val)突变为甲硫氨酸(Met)时,会使得个体更不易感染克里米亚-刚果出血热。
但是宿主也会“顾此失彼”
在人类基因组中宿主限制性天然免疫分子TRIM5α是抑制病毒复制的关键性因素之一。TRIM5α对特定病毒的抑制作用通常情况下由其氨基酸序列决定。PtERV(某种古老内源性逆转录病毒)与HIV-1(人类免疫缺陷病毒)是两种传染性病毒。研究者发现在TRIM5α的结构域内的特定区域第三位的氨基酸在不同的灵长类中存在差异,这导致了不同灵长类对PtERV与HIV-1的抑制能力不同。在人类与黑猩猩中,结构域中特定区域第3位的氨基酸为精氨酸R,不同于大猩猩的谷氨酰胺Q。人与黑猩猩的TRIM5α能有效抑制PtERV的复制但不能有效抑制HIV病毒的复制。相反大猩猩的TRIM5α对HIV-1的抑制作用强于对PtERV的抑制作用(图6)。
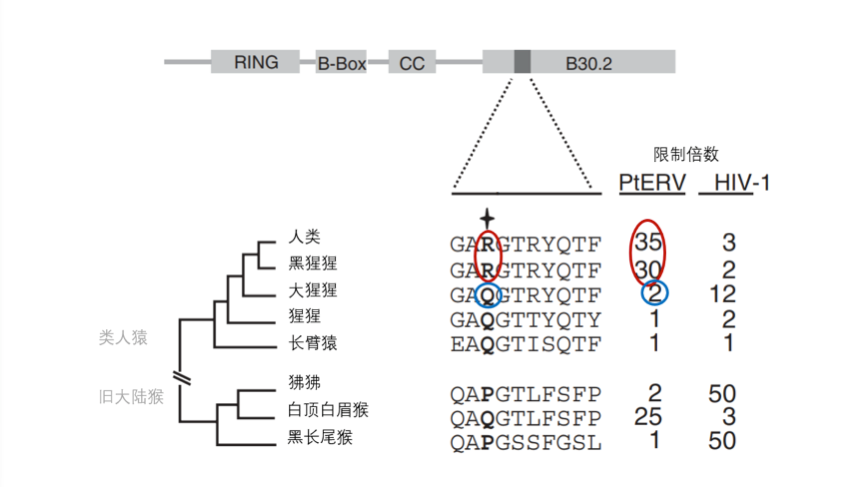
图6.灵长类动物TRIM5α分子的氨基酸差异及对不同病毒的抑制作用(图修订自参考文献[6])
有趣的是,任何事物都存在平衡的状态。自然界为宿主打开一扇“窗”,必然也会同时关上宿主的一道“门”。灵长类的TRIM5α抑制因子对PtERV与HIV-1的抑制作用也存在“平衡”的状态,对一种病毒抑制能力增强,有时会导致对另一种病毒的抑制能力下降。
在病毒与宿主长期共存的演化过程中,双方都建立了一套“攻击”与“防御”的演化机制。客观的说,病毒也是自然界的一种生命形式,它们的演化也遵循自然法则和规律。这些客观规律通过系统的科学研究正在被逐步深入地揭示。我们需要做的是尊重自然界的客观规律,深入揭示自然界的客观规律。这一定能够帮助人类更好的控制与“战胜”病毒!
参考文献:
[1]StephensPR,AltizerS,SmithKF,AguirreAA,BudischakSA,ByersJE,DallasTA,DaviesTJ,DrakeJM,etal.(2016).Themacroecologyofinfectiousdiseases:anewpe,19:1159–1171.
[2]SironiM,CaglianiR,ForniD,ClericiM.(2015).Evolutionaryinsightsintohost–,16:224–236.
[3]DoremalenNV,MiazgowiczKL,PriceSM,BushmakerT,RobertsonS,ScottD,KibbeJ,MclellanJS,ZhuJ,MunsterAJ.(2014).HostSpeciesRestrict,88:9220–9232.
[4]LassoG,MayerSV,,ElliotO,GalindoJAP,KernyuP,RabadanR,HonigB,ShapiraSD.(2019).,178:1526–1541.
[5]DelvesPJ,MartinSJ,BurtonDJ,RoittIM.(2016).EssentialImmunology,13‐Blackwell,Oxford.
[6]KaiserSM,MalikHS,EmermanM.(2007).RestrictionofanextinctretrovirusbythehumanTRIM5α,316:1756–1758.
[7]SawyerSL,WuLI,EmermanM,MalikHS.(2005).PositiveselectionofprimateTRIM5α,102:2832–2837.
[8]LinYT,VermaA,HodgkinsonCP.(2012).Toll-likereceptorsandhumandisease:,13:633–645.
[9]HalehalliRR,NagarajaramHA.(2015).Molecularprinciplesofhumanvirusprotein–,31:1025–1033.
[10]SanzJ,RandolphHE,BarreiroLB.(2018).Geneticandevol,53:28–35.
[11]EnginA,ArslanA,KizildagS,OzturkH,ElaldiN,DokmetasI,BakirM.(2010).Tol,12:1071–1078.
[12]WerlingD,JannOC,OffordV,GlassEJ,CoffeyTJ.(2008).Variationmatters:,30:124–130.